服务热线
178 0020 3020
本期文献
1. 杂交马铃薯的基因组设计
2. 双歧杆菌介导的免疫系统在生命早期印记
3. 易位微生物组合物决定了治疗的HIV感染的免疫学结果
4. 流感疫苗免疫的单细胞表观基因组和转录景观
5. SARS-CoV-2 mRNA疫苗接种诱导针对NTD,RBD和S2的功能多样的抗体
6. 在临床前和人体研究中,单克隆抗体组合REGEN-COV可防止SARS-COV-2突变逃逸
7. 分析SARS-CoV-2 HLA-I肽组揭示来自框外ORF的T细胞表位
8. 局部调节性T细胞反馈回路通过修剪自激活的T细胞来维持免疫稳态
9. CTLA-4依赖性反馈回路中断后肿瘤相关Treg细胞的扩增
10. 分泌的凝溶胶蛋白抑制DNGR-1依赖性交叉呈递和癌症免疫
11. RNA剪接的药理学调节增强了抗肿瘤免疫力
12. GABA接受性小胶质细胞选择性地调控发育抑制回路
13. 2.9Å处RNA聚合酶II预起始复合物的结构定义了初始DNA开放

封面:T细胞介导的免疫在控制SARS-CoV-2感染中起着重要作用,但天然加工和呈递的病毒表位的所有组成部分仍未表征。在本期杂志中,Weingarten-Gabbay等人(3962-3980)发现SARS-CoV-2基因组中的框外开放阅读框(ORF)衍生的病毒表位引发T细胞反应。封面图像是画廊中图片框架的隐喻。它将SARS-CoV-2 T细胞表位分别描绘为来自框内(规范)和框外ORF的花,分别在金框内或外。HLA-I复合物由紫色花表示,并且来自框内和框外ORF的呈递肽的序列在雌蕊中指示。birds说明T细胞与来自框内或框外ORF的HLA-I呈递的肽相互作用,并根据TCR结构着色。画廊窗帘说明这项研究发生在SARS-CoV-2感染的背景下
1. 杂交马铃薯的基因组设计
Genome design of hybrid potato
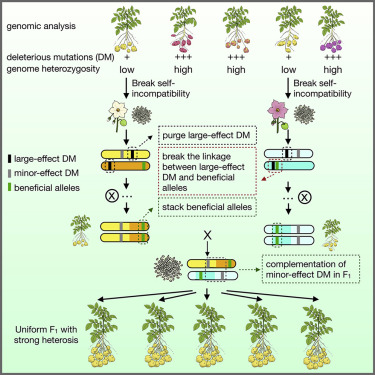
将马铃薯从克隆繁殖的四倍体重新培育成种子繁殖的二倍体杂交马铃薯是农业中的一项重要创新。由于有害的突变,开发高度纯合的近交系仍然是一个挑战,这是培育杂交马铃薯的先决条件。在这里,作者采用基因组设计来开发一代纯净和肥沃的马铃薯品系,从而形成均匀,有活力的F1。作者在基因组设计中应用的指标包括基因组纯合性百分比和起始材料中有害突变的数量,S1群体中分离畸变的数量,推断有益和有害等位基因之间紧密联系断裂的单倍型信息,和亲本系的基因组互补性。本研究将马铃薯育种从缓慢的非累积模式转变为快速迭代模式,从而为农民和消费者带来广泛的利益。
2. 双歧杆菌介导的免疫系统在生命早期印记
Bifidobacteria-mediated immune system imprinting early in life
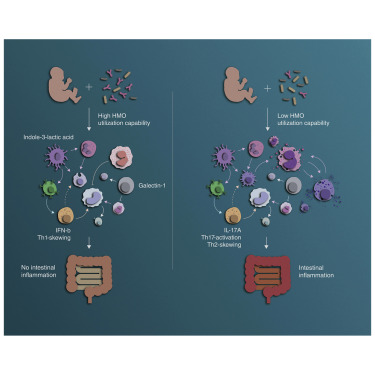
生命早期的免疫-微生物相互作用影响过敏,哮喘和其他炎性疾病的风险。母乳喂养通过向专门的微生物提供营养来指导更健康的免疫微生物关系,从而有利于宿主的免疫系统。这些细菌与人类共同进化,但现在在现代社会中越来越罕见。在这里,作者表明,缺乏双歧杆菌,特别是从宏基因组中利用人乳寡糖(HMO)所需的基因的消耗,与生命早期的全身炎症和免疫失调有关。在给予表达所有HMO利用基因的婴儿双歧杆菌EVC001的母乳喂养的婴儿中,沉默肠T辅助细胞2(Th2)和Th17细胞因子并诱导干扰素β(IFNβ)。EVC001补充婴儿粪便中含有丰富的吲哚乙酸盐和B。婴儿衍生的吲哚-3-乳酸(ILA)在极化期间上调Th2和Th17细胞中的免疫调节半乳糖凝集素-1,在生命的头几个月提供有益微生物和免疫调节之间的功能联系。
3. 易位微生物组合物决定了治疗的HIV感染的免疫学结果
Translocated microbiome composition determines immunological outcome in treated HIV infection
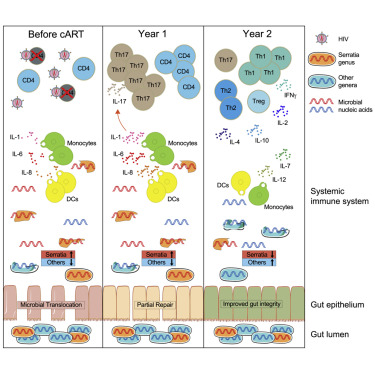
尽管微生物组成波动下游的机制仍然是推测性的,但微生物组对HIV疾病的影响已得到广泛认可。作者在cART启动后两年内检测到易位微生物成分的快速动态变化。一种无偏见的系统生物学方法揭示了由沙雷氏菌与其他细菌属的丰度比变化驱动的两种不同途径。第一年CD4 T细胞数量增加与高沙雷氏菌丰度,促炎先天细胞因子和驱动Th17基因表达特征和恢复粘膜完整性的代谢物有关。随后,沙雷氏菌丰度的降低和先天细胞因子的下调允许重建系统性T细胞稳态,从而促进Th1和Th2基因表达特征的恢复。对其他三个地理上不同的治疗HIV感染队列的分析建立了更普遍的原则,即易位微生物物种的多样性和组成的变化影响全身炎症并因此影响CD4T细胞恢复。
4. 流感疫苗免疫的单细胞表观基因组和转录景观
The single-cell epigenomic and transcriptional landscape of immunity to influenza vaccination
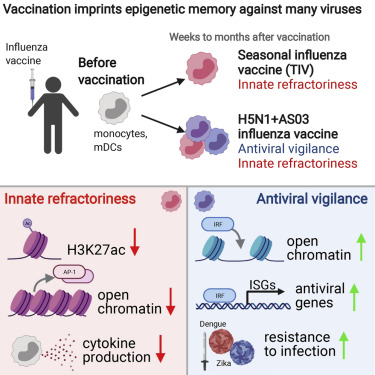
新出现的证据表明表观基因组在免疫中的基本作用。在这里,作者绘制了单细胞水平上人类流感疫苗免疫的表观基因组和转录景观。针对季节性流感的疫苗接种诱导单核细胞和骨髓树突细胞(mDC)中H3K27ac的持续减少,这与细胞因子对Toll样受体刺激的反应受损有关。单细胞ATAC-seq分析揭示了单核细胞的表观基因组学上不同的亚群,接种后AP-1靶向基因座的染色质可及性降低。在用AS03佐剂化的H5N1大流行性流感疫苗接种疫苗时观察到类似的效果。然而,该疫苗还刺激单核细胞和mDC中干扰素应答因子(IRF)基因座的染色质可及性持续增加。这与抗病毒基因的表达升高和对无关的寨卡病毒和登革热病毒的抗性增强有关。这些结果表明疫苗接种刺激先天免疫系统的持续表观基因组重塑,并揭示AS03作为表观遗传佐剂的潜力。
5. SARS-CoV-2 mRNA疫苗接种诱导针对NTD,RBD和S2的功能多样的抗体
SARS-CoV-2 mRNA vaccination induces functionally diverse antibodies to NTD, RBD, and S2
在这项研究中,作者分析了疫苗诱导的多克隆抗体以及来自接受SARS-CoV-2刺突mRNA疫苗的个体的浆母细胞衍生的mAb。疫苗接种者中的多克隆抗体应答是稳健的,与自然感染后观察到的相当或超过。然而,接种疫苗后与中和抗体结合的比例大于自然感染后的比例,并且在单克隆水平上,作者发现大多数疫苗诱导的抗体不具有中和活性。作者还发现针对SARS-CoV-2刺突的NTD和RBD以及针对季节性人冠状病毒OC43和HKU1刺突的原始抗原性sin样骨架的mAb的共同优势。取消了针对携带E484K的临床病毒分离物的NTD-mAb而非RBD-mAb的中和活性以及NTD的广泛变化,表明一定比例的疫苗诱导的RBD结合抗体可以提供针对携带病毒变体的实质性保护。单个E484K RBD突变。
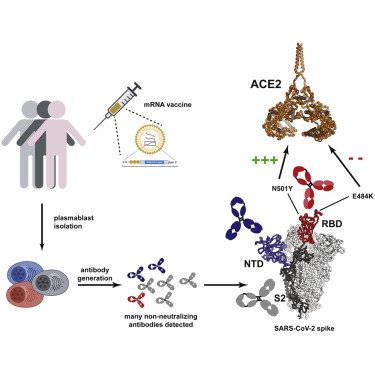
6. 在临床前和人体研究中,单克隆抗体组合REGEN-COV可防止SARS-COV-2突变逃逸
The monoclonal antibody combination REGEN-COV protects against SARS-CoV-2 mutational escape in preclinical and human studies
针对SARS-CoV-2的单克隆抗体是针对COVID-19的临床验证治疗选择。由于迅速出现的病毒突变体正成为抗击全球大流行的下一个主要问题,这些治疗性治疗必须提供针对循环变体的覆盖,并且不会促进治疗诱导的紧急抗性的发展。为此,作者调查了刺突蛋白的序列多样性,并监测了在用两种抗体组合REGEN-COV治疗的COVID-19患者中发现的SARS-COV-2分离株中病毒变体的出现,以及在临床前体外研究中使用单一,双重或三重抗体组合,以及使用REGEN-COV或单单克隆抗体治疗的仓鼠体内研究。作者的研究表明,REGEN-COV中非竞争性抗体的组合提供针对所有当前关注/感兴趣的SARS-COV-2变体的保护,并且还防止新变体的出现及其在临床环境中潜在地接种到群体中。
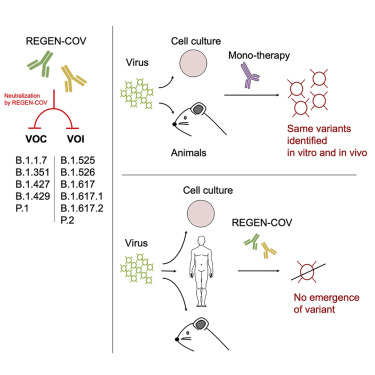
7. 分析SARS-CoV-2 HLA-I肽组揭示来自框外ORF的T细胞表位
Profiling SARS-CoV-2 HLA-I peptidome reveals T cell epitopes from out-of-frame ORFs
T细胞介导的免疫在控制SARS-CoV-2感染中起重要作用,但I类人白细胞抗原(HLA-I)上天然加工和呈递的病毒表位的所有组成成分仍未表征。在这里,作者使用质谱法在感染后不同时间报告两种细胞系中SARS-CoV-2的第一个HLA-I免疫肽组。作者发现HLA-I肽不仅来源于规范的开放阅读框(ORF),而且来源于目前疫苗未捕获的刺突和核衣壳中的内部框外ORF。来自框外ORF的一些肽在人源化小鼠模型和具有COVID-19的个体中引发T细胞应答,其超过对经典肽的应答,包括迄今为止报道的一些最强表位。感染细胞的全蛋白质组分析显示早期表达的病毒蛋白对HLA-I呈递和免疫原性贡献更大。这些生物学见解以及框架外ORF表位的发现将有助于选择用于免疫监测和疫苗开发的肽。
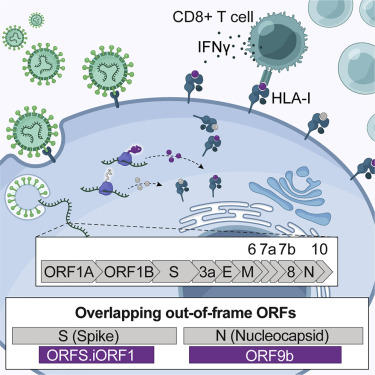
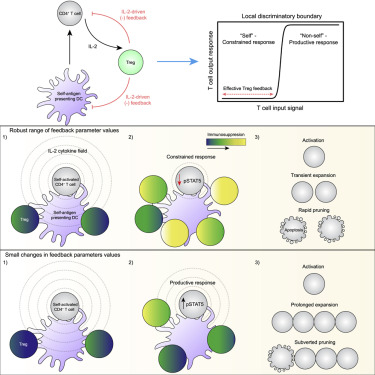
8. 局部调节性T细胞反馈回路通过修剪自激活的T细胞来维持免疫稳态
A local regulatory T cell feedback circuit maintains immune homeostasis by pruning self-activated T cells
一部分成熟T细胞可被外周自身抗原激活,可能引发宿主自身免疫。作者通过将高分辨率多路复用和体积成像与计算建模相结合,研究了未受干扰的组织环境中自激活T细胞的稳态控制。在淋巴结中,自激活的T细胞产生白细胞介素(IL)-2,其增强局部调节性T细胞(Treg)增殖和抑制功能。由此产生的微域相互约束破坏效应器响应所需的输入,包括CD28共刺激和IL-2信号传导,构成负反馈电路。由于这些局部限制,自激活的T细胞经历短暂的克隆扩增,随后快速死亡(“修剪”)。计算模拟和实验操作揭示了反馈机器的定量限制:Treg微区密度或功能的适度降低产生了控制中的非线性分解,使得自激活的T细胞能够破坏修剪。这种微调的旁分泌反馈过程不仅可以加强免疫稳态,还可以在自身免疫和宿主保护性T细胞反应之间建立清晰的界限。
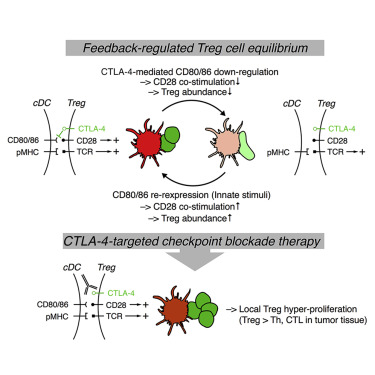
9. CTLA-4依赖性反馈回路中断后肿瘤相关Treg细胞的扩增
Expansion of tumor-associated Treg cells upon disruption of a CTLA-4-dependent feedback loop
Foxp3+T调节(Treg)细胞促进免疫肿瘤耐受,但如何在肿瘤微环境(TME)中调节其免疫抑制功能仍然未知。在这里,作者使用活体显微镜来表征为肿瘤浸润Treg细胞提供关键激活信号的细胞相互作用。作者发现多克隆Treg细胞库被预富集以识别由肿瘤相关的常规树突细胞(cDC)呈递的抗原。不稳定的cDC接触足以维持Treg细胞功能,而T辅助细胞在稳定的相互作用过程中被激活。接触不稳定性是由Treg细胞本身介导的CDC上共刺激B7家族蛋白的CTLA-4依赖性下调引起的。CTLA-4阻断在TME中触发CD28依赖性Treg细胞过度增殖,并且需要伴随的Treg细胞失活来实现肿瘤排斥。因此,Treg细胞通过CTLA-4和CD28依赖性反馈环自我调节,该反馈环将其群体大小调整为局部共刺激的量。其通过CTLA-4阻断的破坏可能会抵消癌症患者的治疗益处。
10. 分泌的凝溶胶蛋白抑制DNGR-1依赖性交叉呈递和癌症免疫
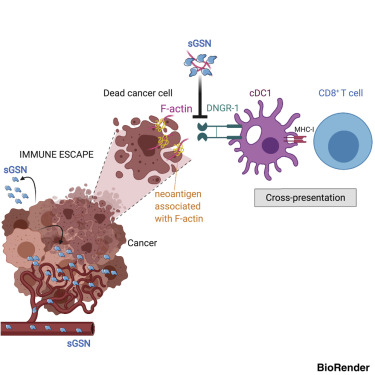
Secreted gelsolin inhibits DNGR-1-dependent cross-presentation and cancer immunity
通过1型常规树突细胞(cDC1)交叉呈递来自死亡肿瘤细胞的抗原被认为是抗癌CD8+T细胞引发的基础。cDC1表达高水平的DNGR-1(又称CLEC9A),该受体与死细胞碎片暴露的F-肌动蛋白结合并促进相关抗原的交叉呈递。在这里,作者显示分泌的凝溶胶蛋白(sGSN),一种细胞外蛋白,降低DNGR-1与F-肌动蛋白的结合和cDC1s交叉呈递死细胞相关抗原。缺乏sGsn的小鼠显示出对可移植肿瘤的DNGR-1依赖性抗性增加,尤其是表达与肌动蛋白细胞骨架相关的新抗原的小鼠,并且对癌症免疫疗法表现出更高的反应性。在人类癌症中,较低水平的肿瘤内sGSN转录物以及与肌动蛋白细胞骨架相关的蛋白质中的突变的存在与抗癌免疫的特征和增加的患者存活相关。作者的研究结果揭示了交叉呈递抑制抗肿瘤CD8+T细胞应答的癌抗原的天然屏障。
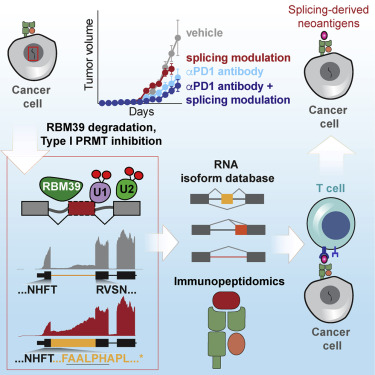
11. RNA剪接的药理学调节增强了抗肿瘤免疫力
Pharmacologic modulation of RNA splicing enhances anti-tumor immunity
尽管DNA中的突变是确定对免疫检查点阻断的响应的新抗原的最佳研究来源,但癌细胞内RNA剪接的改变可类似地导致新表位产生。然而,尚未测试这种剪接衍生表位的内源性抗原性和临床潜力。在这里,作者证明通过特定药物类别的剪接的药理学调节产生真正的新抗原并引发抗肿瘤免疫,增强检查点免疫疗法。剪接调节以依赖于宿主T细胞和呈递在肿瘤MHC I类上的肽的方式抑制肿瘤生长并增强检查点阻断。剪接调节诱导肿瘤类型的定型剪接变化,改变MHC I结合的免疫肽组以产生剪接衍生的新表位,其在体内触发抗肿瘤T细胞应答。这些数据明确地将剪接调节鉴定为未开发的免疫原性肽来源,并提供增强对易于翻译成临床的检查点阻断的响应的手段。
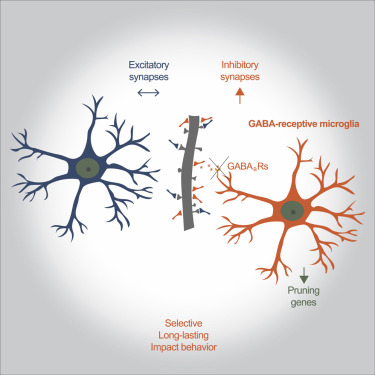
12. GABA接受性小胶质细胞选择性地调控发育抑制回路
GABA-receptive microglia selectively sculpt developing inhibitory circuits
小胶质细胞是大脑的常驻免疫细胞,已成为突触细化和大脑布线的关键调节因子。然而,在发育过程中不同突触类型的重塑是否由专门的小胶质细胞介导是未知的。在这里,作者显示GABA接受小胶质细胞在小鼠出生后发育的关键窗口期间选择性地与抑制性皮质突触相互作用。GABA在这些专门的小胶质细胞内启动转录突触重塑程序,从而塑造抑制性连接而不影响兴奋性突触。小胶质细胞内GABAB受体的消融损害了这一过程并导致行为异常。这些发现表明,大脑布线依赖于匹配的神经元和神经胶质细胞类型之间的选择性通信。
13. 2.9Å处RNA聚合酶II预起始复合物的结构定义了初始DNA开放
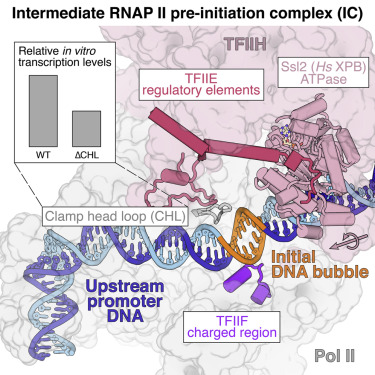
Structure of RNA polymerase II pre-initiation complex at 2.9 Å defines initial DNA opening
转录起始需要组装RNA聚合酶II(Pol II)预起始复合物(PIC)并打开启动子DNA。在这里,作者提出了酵母PIC长期寻求的高分辨率结构,并定义了初始DNA开放的机制。作者将PIC捕获在中间状态,该状态包含位于TATA盒下游30–35个碱基对的半圈开放DNA。最初打开的DNA区域的两侧是聚合酶“钳头环”和TFIIF“带电区域”,它们都有助于启动子启动的转录。TFIIE通过支撑钳头环和调节TFIIH转位酶来促进启动。然后初始DNA气泡沿上游方向延伸,导致开放的启动子复合物并实现起始位点扫描和RNA合成。这种独特的DNA开放机制可能允许比Pol I和Pol III系统更复杂的调节。
本期链接:https://www.cell.com/cell/issue?pii=S0092-8674(20)X0016-X
附件