服务热线
178 0020 3020
每期文献
1 新型蝙蝠冠状病毒的鉴定揭示了 SARS-CoV-2 和相关病毒的进化起源
2 Spike基因的选择性扫描驱动了 SARS-CoV-2 人类适应
3 针对 SARS-CoV-2 变体和 sarbecovirus 的结构引导 T 细胞疫苗设计
4 泛保护性抗α病毒人抗体靶向保守的E1蛋白表位
5 治疗性α病毒交叉反应性E1人抗体抑制病毒流出
6 人TBK1缺陷导致由TNF诱导的细胞死亡驱动的自身炎症
7 红细胞线粒体滞留触发人类SLE中的髓样依赖性I型干扰素
8 PFKL的选择性激活抑制吞噬氧化爆发
9 通过Ragulator-Rag-mTORC1途径控制gasdermin D寡聚化和pyroptosis

封面:抗菌药物针对必需细菌基因的产物。然而,传统遗传方法所提供的重要性的全有或全无定义未能辨别出最具吸引力的抗生素靶标:那些部分抑制导致严重健康成本的抗生素靶标。在本期中,Bosch等人(4579-4592)描述了基因组规模的CRISPR干扰平台的开发,该平台可以精确调节基因表达并模拟部分抑制。这个被称为基因脆弱性的概念重新定义了基因的重要性,并为优先考虑基于目标的药物发现目标提供了路线图。封面图片表明,来自纽约市brownstones的基因脆弱性分析可以为结核病及其他药物开发打开机会之窗。
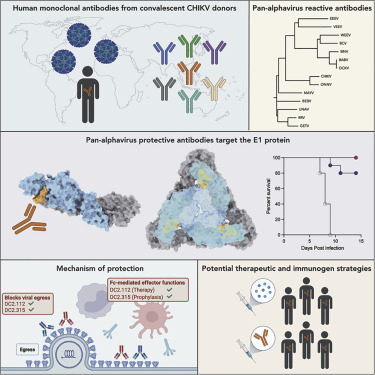
4 泛保护性抗α病毒人抗体靶向保守的E1蛋白表位
Pan-protective anti-alphavirus human antibodies target a conserved E1 protein epitope
蚊子传播的病原体甲病毒正在出现,导致人类肌肉骨骼和神经系统疾病。尽管已经描述了抑制个体α病毒的中和抗体,但是尚未报道针对致关节炎和脑炎α病毒的广泛反应性抗体。在这里,我们确定DC2.112和DC2.315,两种泛保护但中和不良的人单克隆抗体(mAb),它们与感染了致关节炎和脑炎α病毒的细胞表面上的病毒抗原狂热结合。这些mAb在融合肽附近和内部的E1蛋白的结构域II中接合保守表位。用DC2.112或DC2.315处理通过多种机制保护小鼠免受致关节炎(基孔肯雅热和马亚罗)和脑炎(委内瑞拉,东部和西部马脑炎)α病毒的感染,包括抑制病毒出口和单核细胞依赖性Fc效应子功能。这些发现定义了由弱中和但保护性抗体识别的保守表位,其可以靶向泛α病毒免疫疗法和疫苗设计。
5 治疗性α病毒交叉反应性E1人抗体抑制病毒流出
Therapeutic alphavirus cross-reactive E1 human antibodies inhibit viral egress
甲病毒引起严重的关节炎或脑炎疾病。E1结构糖蛋白在这些病毒中高度保守并介导病毒与宿主细胞的融合。然而,人们对免疫中E1蛋白的抗体反应的作用知之甚少。我们从天然EEEV感染的幸存者中分离出具有不同模式的α病毒识别的E1特异性人单克隆抗体(mAb)(范围从东部马脑炎病毒[EEEV]-特异于α病毒交叉反应)。抗体结合模式和表位作图实验基于通过pH依赖性机制暴露糖蛋白上的表位或在病毒流出之前在细胞表面上呈递,鉴定了E1反应性的差异。这些mAb的体内治疗功效对应于体外病毒出口抑制的效力,并且不需要Fc介导的效应子功能来治疗皮下EEEV攻击。这些研究揭示了对α病毒E1蛋白的广泛和保护性抗体应答的分子基础。
6 人TBK1缺陷导致由TNF诱导的细胞死亡驱动的自身炎症
Human TBK1 deficiency leads to autoinflammation driven by TNF-induced cell death
TANK结合激酶1(TBK1)调节IFN-1,NF-κB和TNF诱导的RIPK1依赖性细胞死亡(RCD)。在小鼠中,TBK1的双等位基因缺失在胚胎上是致命的。我们从三个不相关的近亲家庭中发现了四个人,年龄分别为32、26、7和8,它们在TBK1中具有纯合功能丧失突变。所有四名患者均患有慢性和全身性自身炎症,但未患有严重的病毒感染。我们证明TBK1损失通过RIG-I/MDA5导致亚型但足够的IFN-1诱导,而系统通过NF-κB保留几乎完整的IL-6诱导。自身炎症由TNF诱导的RCD驱动,因为患者来源的成纤维细胞在体外经历更高的坏死性凋亡率,并且体外外周血中CC3升高。用抗TNF治疗抑制了基线循环炎症特征并改善了体内临床状况。这些发现突出了IFN-I反应的可塑性,并强调了TBK1在调节RCD中的主要作用。

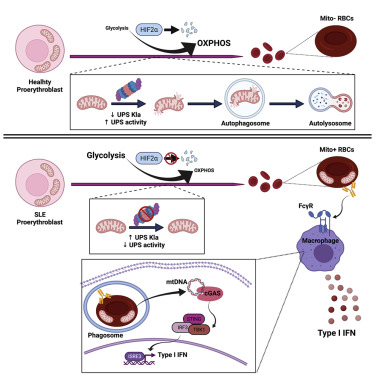
7 红细胞线粒体滞留触发人类SLE中的髓样依赖性I型干扰素
Erythroid mitochondrial retention triggers myeloid-dependent type I interferon in human SLE
新出现的证据支持线粒体功能障碍导致系统性红斑狼疮(SLE)发病机制。在这里,我们显示程序性线粒体去除,哺乳动物红细胞生成的标志,在SLE中是有缺陷的。具体而言,我们证明在人类红细胞成熟过程中,缺氧诱导因子(HIF)介导的代谢开关负责泛素-蛋白酶体系统(UPS)的激活,其在自噬去除线粒体之前并且是必需的。该途径中的缺陷导致SLE患者中携带线粒体(Mito+RBC)的红细胞(RBC)的积累并且与疾病活动相关。Mito+RBC的抗体介导的内化通过激活巨噬细胞中的cGAS诱导I型干扰素(IFN)产生。因此,携带Mito+RBC和调理抗体的SLE患者显示出最高水平的血液IFN刺激基因(ISG)特征,这是SLE的显着特征。
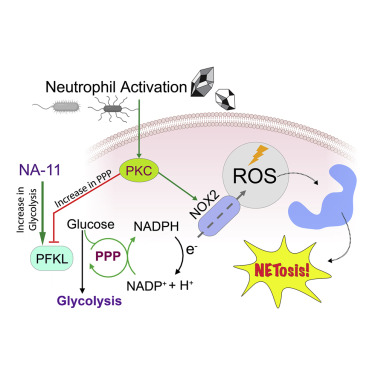
8 PFKL的选择性激活抑制吞噬氧化爆发
Selective activation of PFKL suppresses the phagocytic oxidative burst
在嗜中性粒细胞中,通过戊糖磷酸途径产生的烟酰胺腺嘌呤二核苷酸磷酸(NADPH)促进NADPH氧化酶NOX2产生活性氧以杀死入侵的病原体。然而,过度的NOX2活性会加剧炎症,如急性呼吸窘迫综合征(ARDS)。在这里,我们使用两种无偏化学蛋白质组学策略来显示小分子LDC7559或更有效设计的类似物NA-11通过激活糖酵解酶磷酸果糖激酶-1肝型(PFKL)来抑制嗜中性粒细胞中NOX2依赖性氧化爆发并抑制通过戊糖磷酸途径的通量。因此,用NA-11处理的嗜中性粒细胞具有降低的NOX2依赖性输出,包括嗜中性粒细胞死亡(NETosis)和组织损伤。PFKL的高分辨率结构证实了NA-11与AMP/ADP变构激活位点的结合,并解释了为什么NA-11不能激动磷酸果糖激酶-1血小板型(PFKP)或肌肉型(PFKM)。因此,NA-11代表选择性激活PFKL的工具,PFKL是免疫细胞中表达的主要磷酸果糖激酶-1同种型。
9 通过Ragulator-Rag-mTORC1途径控制gasdermin D寡聚化和pyroptosis
Control of gasdermin D oligomerization and pyroptosis by the Ragulator-Rag-mTORC1 pathway
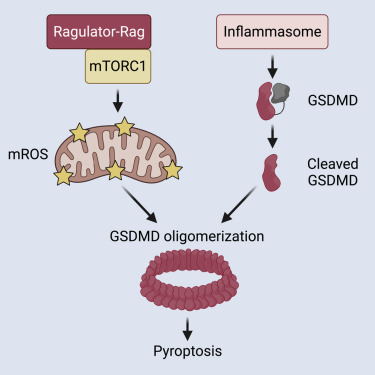
pyroptosis的过程由炎性体和称为gasdermin D(GSDMD)的下游效应子介导。在被炎性体相关半胱天冬酶切割后,GSDMD的N-末端结构域形成促进细胞溶解的膜孔。许多蛋白质促进GSDMD切割,但已知在GSDMD切割后孔形成不需要任何蛋白质。在这里,我们报告了一个前向遗传筛选,确定Ragulator-Rag复合物是巨噬细胞中GSDMD孔形成和pyroptosis所必需的。机理分析显示Ragulator Rag不是炎性体激活后GSDMD切割所必需的,而是促进质膜中GSDMD寡聚化。GSDMD寡聚化和孔形成的缺陷可以通过刺激活性氧(ROS)产生的线粒体毒物来挽救,并且ROS调节影响炎性体途径促进GSDMD切割下游的孔形成的能力。这些发现揭示了免疫(炎性体GSDMD)和代谢(Ragulator Rag)的关键调节因子之间意想不到的联系。
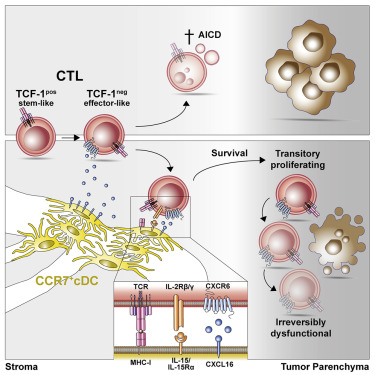
10 CXCR6定位细胞毒性T细胞以在肿瘤微环境中接收关键存活信号
CXCR6 positions cytotoxic T cells to receive critical survival signals in the tumor microenvironment
针对肿瘤的细胞毒性T淋巴细胞(CTL)应答由自我更新但也产生效应样细胞的干样记忆细胞维持。后者逐渐失去其抗肿瘤活性并获得表观遗传学固定的功能减退状态,导致肿瘤耐受。在这里,我们显示干样转化为效应样CTL涉及主要的趋化重编程,包括趋化因子受体CXCR6的上调。该受体将效应子样CTL定位在肿瘤基质的离散血管周围生态位中,该生态位被表达CXCR6配体CXCL16的CCR7+树突细胞(DC)密集占据。CCR7+DC还表达并反式呈递存活细胞因子白细胞介素-15(IL-15)。CXCR6表达和IL-15反式呈递对于肿瘤微环境中效应样CTL的存活和局部扩增至关重要,以在进展为不可逆功能障碍之前使其抗肿瘤活性最大化。这些观察揭示了确定抗肿瘤免疫应答的大小和结果的细胞和分子检查点。
11 核糖体ADP-核糖基化抑制翻译并维持癌症中的蛋白质稳态
Ribosome ADP-ribosylation inhibits translation and maintains proteostasis in cancers
翻译缺陷导致蛋白质表达的改变,这些蛋白质可以作为癌症形成的驱动因素。在这里,我们显示细胞溶质NAD+合成通过调节翻译和维持蛋白质稳态在卵巢癌中起重要作用。NMNAT-2(一种胞质NAD+合酶)的表达在卵巢癌中高度上调。NMNAT-2支持单(ADP-核糖基)转移酶(MART)PARP-16的催化活性,其单(ADP-核糖基)ates(MARylates)核糖体蛋白。NMNAT-2或PARP-16的消耗导致抑制马里酸化,增加多核糖体结合并增强特定mRNA的翻译,其翻译的蛋白质产物的聚集和卵巢癌细胞的生长减少。此外,核糖体蛋白(例如RPL24和RPS6)的马里酸化通过稳定eIF6与核糖体的结合来抑制多核糖体组装。总的来说,我们的研究结果表明,核糖体MARylation通过微调蛋白质合成水平和防止有毒蛋白质聚集来促进癌症中的蛋白质稳态。

12 ELAVL4,剪接和谷氨酸能功能障碍先于MAPT突变脑类器官中的神经元丢失
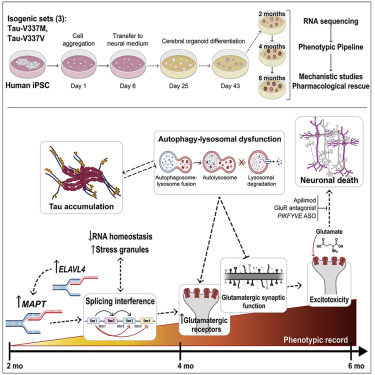
ELAVL4, splicing, and glutamatergic dysfunction precede neuron loss in MAPT mutation cerebral organoids
由于MAPT突变引起的额颞叶痴呆(FTD)通过未知机制导致tau的病理积累和谷氨酸能皮质神经元死亡。我们使用表达tau-V337M的人诱导多能干细胞(iPSC)衍生的脑类器官和等基因校正的对照来发现早期改变,因为神经变性之前的突变。在2个月时,突变类器官显示MAPT,谷氨酸能信号传导途径和调节剂(包括RNA结合蛋白ELAVL4)的上调表达和增加的应激颗粒。在接下来的4个月中,突变类器官积累了剪接变化,自噬功能破坏以及tau和P-tau-S396的积累。到6个月时,如FTD患者所见,tau-V337M类器官显示出谷氨酸能神经元的特异性丧失。突变的神经元对谷氨酸毒性敏感,可以通过PIKFYVE激酶抑制剂apilimod药理挽救。我们的结果证明了神经退行性变之前的一系列事件,揭示了与谷氨酸信号传导相关的分子途径是FTD治疗干预的潜在靶标。
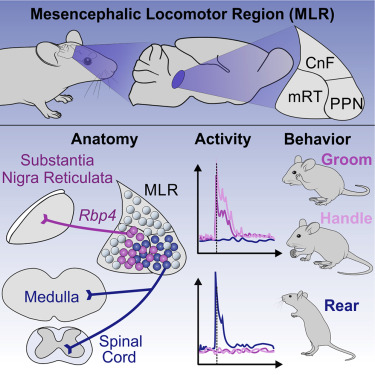
13 中脑运动区身体行为的功能多样性
Functional diversity for body actions in the mesencephalic locomotor region
中脑运动区(MLR)是一个关键的中脑中心,在运动中起作用。尽管针对治疗抵抗性帕金森病(PD)进行了广泛的研究和临床试验,但其功能的争论依然存在。在这里,我们揭示了在控制身体运动中具有不同作用的功能多样的神经元群体的存在。我们确定了两个空间混合的谷氨酸能人群可通过轴突投影,小鼠遗传学,神经元活动概况和运动功能分开。大多数脊柱投射的MLR神经元编码全身行为饲养。功能丧失和功能获得光遗传学扰动实验为这些神经元建立了控制身体伸展的功能。相反,Rbp4转基因阳性MLR神经元向基底神经节上行投射,优先编码处理和梳理的前肢行为,并在调节运动中发挥作用。因此,MLR含有由投射目标分层的谷氨酸能神经元亚群,其在不限于运动的作用控制中表现出作用。
本期链接:https://www.cell.com/cell/issue?pii=S0092-8674(20)X0018-3
附件