服务热线
178 0020 3020
本期文献
1 SARS-CoV-2感染人类成人供体眼和hESC衍生的眼上皮细胞
2 使用类器官和单细胞测序探索人泪腺
3 单个角膜干细胞的双光子实时成像揭示了角膜缘生态位的分隔组织
4 离散的角膜缘上皮干细胞群介导角膜稳态和伤口愈合
5 从体细胞突变推断人类前列腺的发育,成熟和维持
6 HectD1通过协调核糖体组装和蛋白质合成来控制造血干细胞再生
7 供体细胞记忆赋予直接转化细胞的亚稳态
8 涡虫干细胞指定命运,但在细胞周期中保持效力
9 靶向microRNA介导的基因抑制限制了骨骼肌间充质基质细胞的脂肪形成转化

封面:这个问题的特点是几项研究应用先进的技术,以更好地了解眼睛的生物学。其中包括两项研究角膜缘干细胞和生态位动态的研究,一篇研究SARS-CoV-2如何感染人眼上皮的论文,以及使用3D细胞培养工具制作人和小鼠泪腺类器官的封面故事。Bannier-Hélaouët等人(1221-1232)使用化学刺激体外衍生的泪腺来诱导其内容物的肿胀和释放。封面图像显示类器官“脱落”在封面上。
1 SARS-CoV-2感染人类成人供体眼和hESC衍生的眼上皮细胞
SARS-CoV-2 infects human adult donor eyes and hESC-derived ocular epithelium
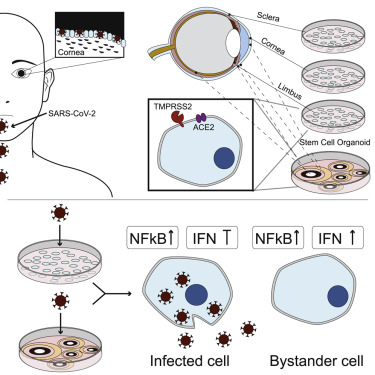
SARS-CoV-2大流行造成了无与伦比的全球行为破坏和严重的生命损失。为了尽量减少SARS-CoV-2传播,了解所有可能进入途径的感染机制至关重要。虽然气溶胶传播被认为是主要的传播途径,但已在眼液中检测到病毒颗粒,这表明眼睛可能是病毒进入的脆弱点。为此,我们在死后COVID-19患者眼表组织中证实了SARS-CoV-2进入因子和抗原表达,并观察到尸体样品和眼类器官培养物中的生产性病毒复制,最显着的是在角膜缘区域。离体感染的眼表细胞和hESC衍生的眼培养物的转录分析揭示了感染细胞中NF-κB的强烈诱导以及I/III型干扰素信号传导的减少。这些数据一起表明眼睛可以直接被SARS-CoV-2感染,并暗示角膜缘作为病毒进入的门户。
2 使用类器官和单细胞测序探索人泪腺
Exploring the human lacrimal gland using organoids and single-cell sequencing
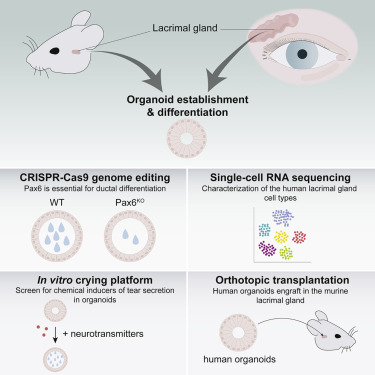
泪腺对于润滑和保护眼睛至关重要。泪液产生,组成或释放的破坏导致干眼症,引起不适和眼表损伤。在这里,我们描述了为小鼠和人类泪腺建立长期3D器官培养条件。类器官可以在多个月内扩展并概括泪管的形态和转录特征。CRISPR-Cas9介导的基因组编辑揭示了眼睛发育的主要调节因子Pax6是成人泪腺细胞分化所必需的。我们通过提供人泪腺组织和类器官的单细胞图谱来解决泪腺的细胞异质性。最后,人泪腺类器官表征响应于神经递质的泪液分泌过程,并且可以在小鼠原位移植后移植并产生成熟的泪液产物。总之,这项研究为研究泪腺的(病理)生理学提供了一个实验平台。
3 单个角膜干细胞的双光子实时成像揭示了角膜缘生态位的分隔组织
Two-photon live imaging of single corneal stem cells reveals compartmentalized organization of the limbal niche
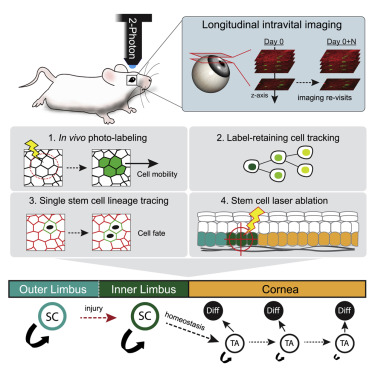
支持成人器官的常驻干细胞的功能异质性尚不完全清楚。在这里,我们直接可视化活小鼠眼睛中的角膜缘并识别离散的干细胞生态位隔室。通过记录单个干细胞及其后代的生命周期,我们直接分析它们的命运并显示它们在组织内的位置可以预测它们的分化状态。内缘中的干细胞主要经历对称分裂,并且需要维持支持角膜稳态的瞬时祖细胞群。使用原位光标记,我们捕获了他们的后代离开生态位,然后一致地向心移动。长期牵连的慢速循环干细胞在功能上是不同的,并且在体内平衡期间显示局部克隆动力学,但是可以促进损伤后的角膜再生。这项研究表明功能多样的干细胞群体的分区组织如何支持成人器官的维持和再生。
4 离散的角膜缘上皮干细胞群介导角膜稳态和伤口愈合
Discrete limbal epithelial stem cell populations mediate corneal homeostasis and wound healing
角膜的可及性和透明度允许稳健的干细胞标记和体内细胞命运映射。传统上,更新角膜的角膜缘上皮干细胞(LSCs)被视为罕见的缓慢循环细胞,其遵循决定其自我更新或分化的确定性规则。在这里,我们结合单细胞RNA测序和先进的定量谱系追踪深入分析小鼠角膜缘上皮。这些分析揭示了两个LSC群体的共存,这两个LSC群体位于独立且定义明确的子区室中,称为“外部”和“内部”角膜缘。静止的外部LSCs的原始群体参与伤口愈合和边界形成,并且这些细胞受作为生态位的T细胞调节。相反,内部角膜周围角膜缘拥有维持角膜上皮稳态的活跃LSCs。定量分析表明,遵循随机规则和中性漂移动力学,LSC群体丰富。这些结果一起表明离散的LSC群体介导角膜稳态和再生。
5 从体细胞突变推断人类前列腺的发育,成熟和维持
Development, maturation, and maintenance of human prostate inferred from somatic mutations
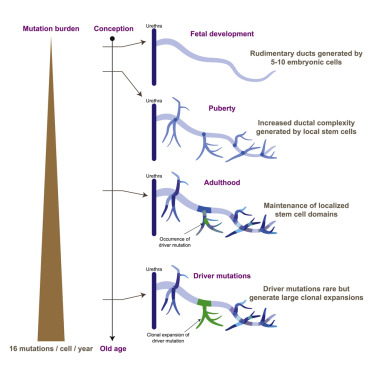
健康人前列腺上皮细胞的克隆动力学和突变负荷与前列腺癌有关。我们对来自8个供体的409个正常前列腺上皮显微切割的全基因组进行了测序,使用59岁男性前列腺中的空间映射的系统发育重建来重建整个生命周期中的组织动力学。体细胞突变稳定积累在∼16个突变/年/克隆,外周率高于尿道周围区域。24-30个独立的腺体亚基在胎儿发育过程中分别由5-10个胚胎细胞建立为基本的导管结构。青春期诱导在发育过程中通过遍布基本导管的局部干细胞形成进一步的侧枝和末端分支。在成人组织维持期间,克隆扩展具有有限的地理范围和最小的迁移。驱动突变在老化的前列腺上皮中很少见,但我们观察到的一个驱动因素产生了相当大的上皮内克隆扩增。利用无偏见的时钟样突变,我们通过胎儿发育,青春期和衰老来定义前列腺干细胞动力学。

6 HectD1通过协调核糖体组装和蛋白质合成来控制造血干细胞再生
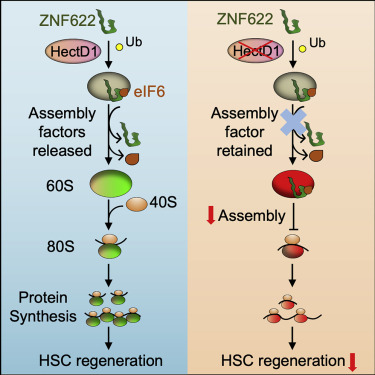
HectD1 controls hematopoietic stem cell regeneration by coordinating ribosome assembly and protein synthesis
核糖体功能受损是一组称为核糖体病的骨髓衰竭综合征的潜在病因。然而,如何调节核糖体仍然知之甚少,以及由于核糖体生物发生缺陷而恢复造血干细胞(HSC)功能丧失的方法。在这里,我们揭示了E3泛素连接酶HectD1在通过核糖体组装和蛋白质翻译调节HSC功能中的作用。缺乏Hectd1的HSC在移植能力和离体维持方面表现出明显的缺陷,同时在压力条件下蛋白质合成和生长速率降低。从机制上讲,HectD1泛素化并降解ZNF622,ZNF622是核糖体60S亚基的装配因子。Hectd1丢失导致ZNF622和抗缔合因子eIF6在60S上积累,导致60S/40S连接缺陷。重要的是,Hectd1缺陷型HSC中的Znf622消耗恢复了核糖体亚基连接,蛋白质合成和HSC重建能力。这些发现强调了泛素协调的核糖体装配在HSC再生中的重要性。
7 供体细胞记忆赋予直接转化细胞的亚稳态
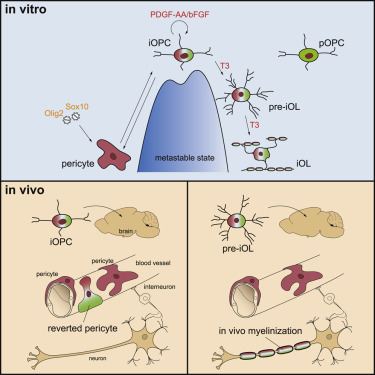
Donor cell memory confers a metastable state of directly converted cells
从体细胞成纤维细胞产生诱导的少突胶质细胞祖细胞(iOPC)是基于细胞的髓鞘疾病治疗策略。然而,iOPC的产生效率低下,并且所得到的iOPC表现出有限的扩增和分化能力。在这里,我们通过将优化的转录因子组合转导到允许的供体表型周细胞中来克服这些限制。周细胞衍生的iOPCs(PC-iOPCs)具有稳定的可扩增性和功能性髓鞘形成,具有高分化能力。然而,出乎意料的是,我们发现PC-iOPCs是亚稳态的,因此它们可以产生具有髓鞘形成能力的少突胶质细胞或以上下文相关的方式恢复其原始身份。PC-iOPCs的表型逆转与其原始转录组和表观基因组的记忆紧密相关。表型逆转可以与这种供体细胞记忆效应断开,并且体内髓鞘形成最终可以通过移植O4+前少突胶质细胞来实现。我们的数据显示供体细胞来源和记忆可以促进直接转化细胞的命运和稳定性。
8 涡虫干细胞指定命运,但在细胞周期中保持效力
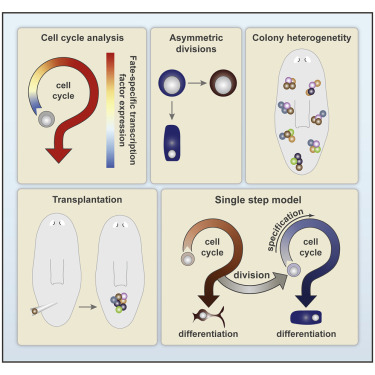
Planarian stem cells specify fate yet retain potency during the cell cycle
通过称为新生细胞的干细胞实现涡虫全身再生。至少一些成神经细胞是单独多能的。成神经细胞也是异质的,具有不同特定命运的特化成神经细胞亚群。成神经细胞的命运规范受命运特异性转录因子(FSTF)表达的调控。在这里,我们发现FSTF表达在成神经细胞S/G2/M细胞周期阶段很常见,但在G1中较少见。我们发现专门的成神经细胞可以分裂产生具有不对称细胞命运的后代,这表明它们可以保留多能性。此外,在所有成神经细胞集落中均不存在已知的成神经细胞类别,这表明多能性不是任何已知类别的专有属性。我们用单细胞移植测试了这种可能性,这表明至少一些专门的成神经细胞可能是克隆形成的。基于这些发现,我们提出了成神经细胞多能性模型,其中成神经细胞可以在细胞周期中经历特化而不丧失效力。
9 靶向microRNA介导的基因抑制限制了骨骼肌间充质基质细胞的脂肪形成转化
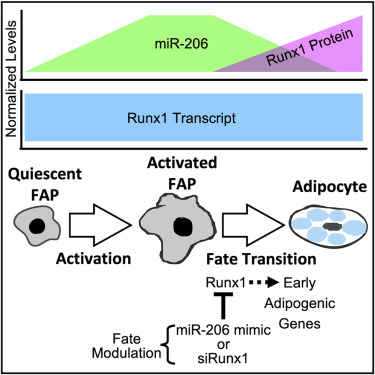
Targeting microRNA-mediated gene repression limits adipogenic conversion of skeletal muscle mesenchymal stromal cells
肌肉营养不良和衰老中可见的肌肉内脂肪沉积会对肌肉功能产生负面影响。构成这些脂肪沉积物的脂肪细胞的起源细胞是间充质基质细胞,纤维生成祖细胞(FAP)。我们揭示了一种分子命运开关,涉及miR-206和转录因子Runx1,控制FAP向脂肪细胞的分化。缺乏miR-206的小鼠在肌肉损伤后表现出增加的脂肪形成。miR-206模拟物消除了FAP的脂肪形成分化。使用标记的microRNA(miRNA)下拉和测序(LAMP-seq),我们将Runx1鉴定为miR-206靶标,miR-206抑制Runx1翻译。在FAP中不存在miR-206时,脂肪形成基因的转录起始位点附近的Runx1占据和这些基因的表达增加。我们证明体内miR-206模拟限制了肌内脂肪浸润。我们的结果提供了深入了解FAP命运决定和骨骼肌中有害脂肪沉积物形成的潜在分子机制的见解。
本期链接:https://www.cell.com/cell-stem-cell/fulltext/S1934-5909(21)00017-5
附件