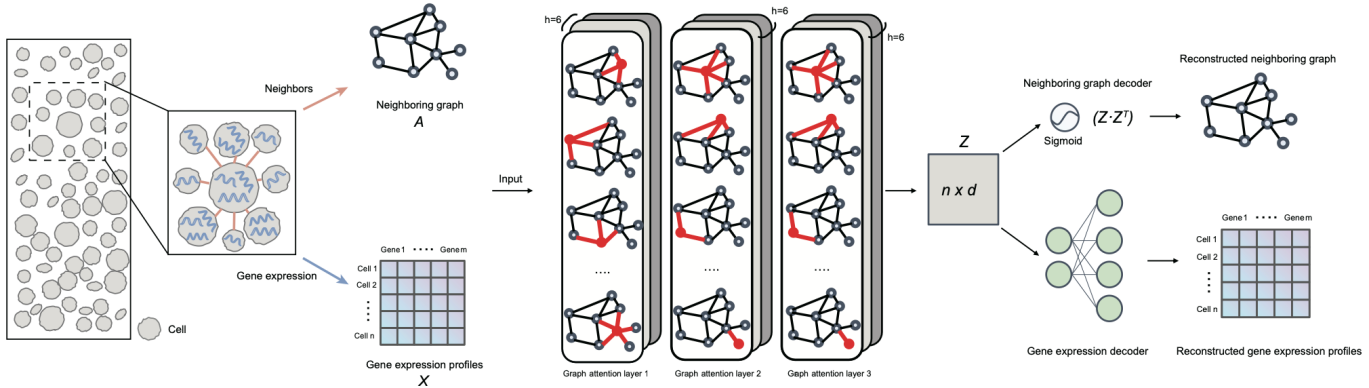
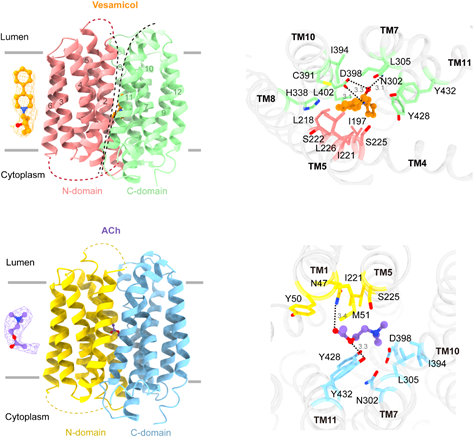
陈苏仁实验室在Protein & Cell发表文章揭示CCDC188基因突变为无头精子症新的致病遗传因素
2024年4月15日,北京师范大学生命科学学院陈苏仁课题组联合国家卫生健康委科学技术研究所王彬彬课题组和北京协和医院李宏军课题组在Protein & Cell(中科院1区,IF=21.1)发表了题为Discovery of CCDC188 gene as a novel genetic target for human acephalic spermatozoa syndrome的文章,研究基于无头精子症患者的全外显子测序和基因敲除小鼠模型揭示了CCDC188蛋白调控精子头尾连接,其基因突变导致无头精子症。该项研究增进了人们对于精子头尾连接的科学认识,并扩展了无头精子症的致病基因谱。

男性不育严重影响人类生殖健康,困扰着世界范围内约6%-8%的育龄男性。无头精子症(Acephalic spermatozoa syndrome, ASS)是一种罕见的但十分严重的男性不育症,表现为精子头尾分离,具有家族遗传特征。2016年,安徽医科大学曹云霞/朱复希团队发现了第一个ASS致病基因SUN5(Sad1 and UNC84 domain containing 5)的变异[1]。SUN5蛋白特异性定位于精子头尾连接处,Sun5基因敲除小鼠雄性不育,其精子表现为头尾分离[2]。2018年,中国科学院动物研究所李卫团队与安徽医科大学曹云霞团队合作报道了第二个ASS致病基因PMFBP1(polyamine modulated factor 1 binding protein 1)的突变[3]。PMFBP1蛋白同样特异性定位于精子的头尾连接处,Pmfbp1基因敲除小鼠的精子也表现为头尾分离[3]。后续许多实验室相继报道了更多ASS患者携带着SUN5和PMFBP1基因变异,证明可它们是ASS主效的致病遗传因素。然而,SUN5和PMFBP1基因突变不能解释所有ASS患者发病的原因,仍有部分ASS患者不携带两者的突变。
本项研究中,联合科研团队开展了不携带SUN5和PMFBP1基因突变的ASS患者的全外显子测序,发现CCDC188基因突变可能是ASS新的致病遗传因素。该名ASS患者(先证者)携带CCDC188基因纯合无义突变(c.937C>T/p.R313*),其父母近亲结婚并为该突变的杂合携带者,其同胞妹妹为正常的野生型,符合常染色体隐性遗传模式。精子巴氏染色、扫描电镜和透射电镜发现患者精液中精子均为无头精子,断裂发生在细胞核和近端中心粒之间(图1)。
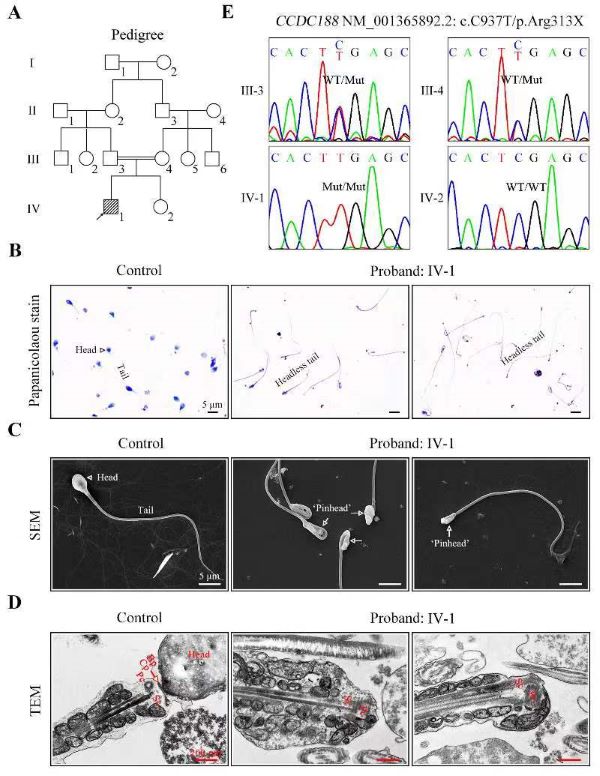
图1. 一名ASS患者携带CCDC188基因纯合无义突变
CCDC188为功能未知蛋白,人类蛋白质图谱(Human Protein Atlas, HPA)数据库显示其特异性表达于睾丸组织中的单倍体精子细胞。为了揭示CCDC188蛋白是否具有调控精子头尾连接的生理功能,研究人员利用CRISPR/Cas9基因编辑技术构建了Ccdc188基因敲除小鼠。Ccdc188基因敲除小鼠雄性不育,其精子头尾分离,证明了CCDC188蛋白的确负责精子头尾连接(图2)。
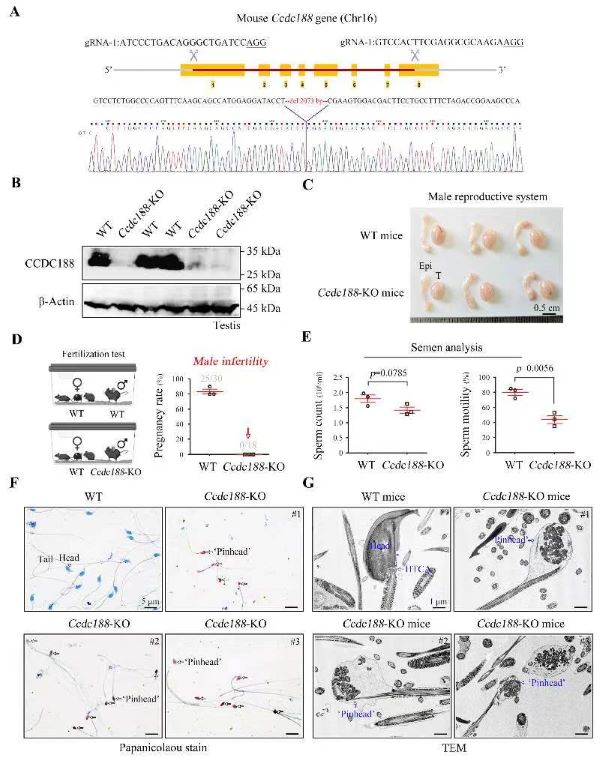
图2.Ccdc188基因敲除小鼠表现为无头精子症
表达研究发现CCDC188蛋白特异性定位于精子头尾连接处。精子头尾连接装置(Head-tail coupling apparatus, HTCA)由植入窝(Implantation fossa)、小头(Capitulum)、节柱(Segmented column)、近端中心粒(Proximal centriole)等超微结构组成。HTCA负责精子头尾连接,HTCA结构缺陷被认为是ASS重要的致病原因之一。Ccdc188基因敲除小鼠睾丸中SUN5和PMFBP1蛋白的表达未受到影响。免疫荧光染色显示精子头尾分离后,SUN5和PMFBP1分别定位于断尾的头和无头的尾。前人研究发现SUN5与PMFBP1并不直接相互作用[3],提示存在其他蛋白负责将SUN5和PMFBP1锚定在一起。本项研究发现CCDC188分别与SUN5和PMFBP1相互作用,在CCDC188存在的情况下,PMFBP1才能够被SUN5免疫共沉淀下来(图3)。
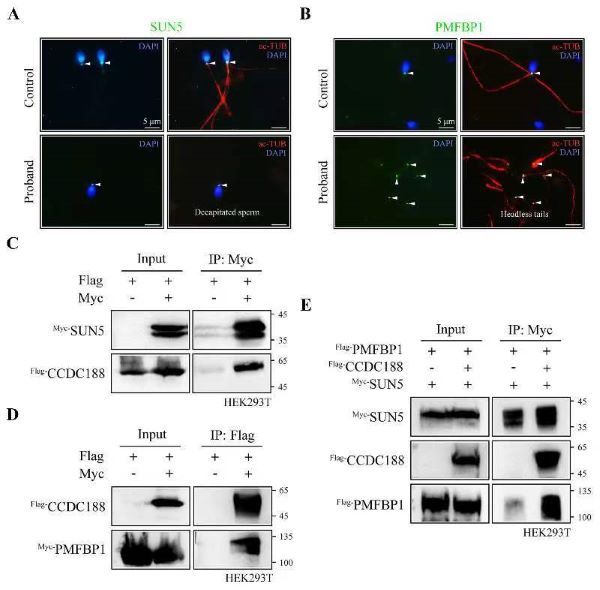
图3.CCDC188蛋白介导SUN5和PMFBP1相互作用
综上所述,本项研究首次在ASS患者中发现了CCDC188基因致病突变,并利用基因敲除小鼠揭示了CCDC188负责精子头尾连接,这可能是通过介导SUN5和PMFBP1的相互作用实现的(图4)。本研究丰富了人们对精子头尾连接的认识,为ASS患者的基因诊断提供了新的靶标。后续研究将从以下两个方面着手:第一,通过开展大规模ASS患者的全外显子测序明确CCDC188基因突变对ASS的贡献度;第二,利用冷冻电子显微镜(Cryo-EM)等技术解析HTCA的超微结构。
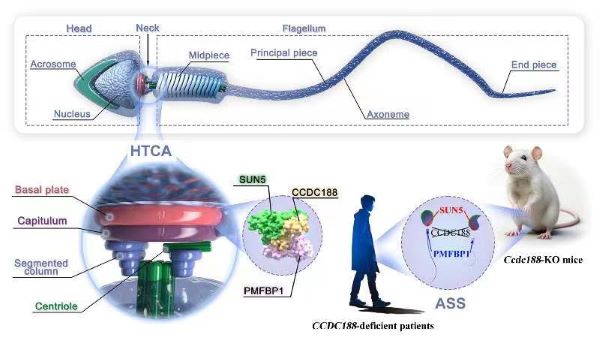
图4. 本研究的模式图
该研究受到国家自然科学基金(32370905)、细胞增殖及调控生物学教育部重点实验室开放基金等资助。
原文链接:
https://academic.oup.com/proteincell/advance-article/doi/10.1093/procel/pwae018/7645618
参考文献:
1. Zhu F, Wang F, Yang X, Zhang J, Wu H, Zhang Z, Zhang Z, He X, Zhou P, Wei Z, Gecz J, Cao Y. Biallelic SUN5 mutations cause autosomal-recessive acephalic spermatozoa syndrome. Am J Hum Genet. 2016; 99(4):942-949.
2. Shang Y, Zhu F, Wang L, Ouyang YC, Dong MZ, Liu C, Zhao H, Cui X, Ma D, Zhang Z, Yang X, Guo Y, Liu F, Yuan L, Gao F, Guo X, Sun QY, Cao Y, Li W. Essential role for SUN5 in anchoring sperm head to the tail. Elife. 2017; 6:e28199.
3. Zhu F, Liu C, Wang F, Yang X, Zhang J, Wu H, Zhang Z, He X, Zhang Z, Zhou P, Wei Z, Shang Y, Wang L, Zhang R, Ouyang YC, Sun QY, Cao Y, Li W. Mutations in PMFBP1 cause acephalic spermatozoa syndrome. Am J Hum Genet. 2018; 103(2):188-199.