服务热线
178 0020 3020
动物细胞培养技术是当今生物工程领域中的前沿技术之一,无论是在研究还是在生产实践方面都对当代生物技术有着重要的影响。近年来随着临床需求的增加,单克隆抗体药物发展迅速,如何提高哺乳动物细胞生产治疗性抗体的产量和质量越来越受到重视。上一篇小编给大家分享了浅谈细胞培养基的基本成分 ,由于细胞培养基是单抗药物生产的关键环节,直接影响到单抗的产量和质量,今天就谈谈细胞培养基的优化,欢迎给位老师给小编指正!
1.培养基的发展
选择合适的细胞培养基进行药物研究,是确保细胞培养活性和蛋白表达的关键。细胞培养基通常包含用于调节pH值的缓冲液, 碳水化合物来源,血清,生长刺激剂和用于细胞代谢功能的矿物质。现今,多种哺乳动物宿主细胞系已用于生产治疗性蛋白质,包括CHO,NS0,BHK,HEK-293和PER-C6。其中CHO细胞作为研究或生产用途最广泛的宿主细胞,所占的使用比例高达50%以上。CHO细胞分泌自身产生的内源性蛋白非常少,但是却可以对成熟的外源性蛋白产生很高表达量。总结起来,CHO细胞适用于进行重组蛋白表达的生物学特性的 优点主要有以下几点:
1.蛋白翻译后的修饰功能:翻译后的修饰功能主要使得蛋白分子在理化特征、分子结构和生物学功能等方面更加接近于天然的蛋白分子。
2.外源重组基因的高效扩增以及高效表达的能力:现在已有二氢叶酸还原酶(dihydrofolate reductase,DHFR)和谷氨酰胺合成酶(glutamine synthetase,GS)基因缺失的CHO变异细胞。这两种基因缺失的变异细胞分别经过氨甲蝶呤(methotrexate,MTX)和蛋氨酸亚氨基带砜(methionine,MSX)的加压筛选后,可以大量增加重组蛋白的基因拷贝数,从而显著提高蛋白的表达水平。
3.产物的胞外分泌功能:由于 CHO 细胞属于成纤维细胞的一种,所以其自身很少分泌内原性蛋白,但是却可以对外源性蛋白进行分泌。此特性使得生产工艺下游的蛋白分离和纯化过程得到了大大的简化。
4.CHO细胞作为成纤维细胞的一种,其既能够进行贴壁培养,也可以进行悬浮培养,并且与其他细胞相比,CHO 细胞可以耐受较高的剪切力和渗透压。
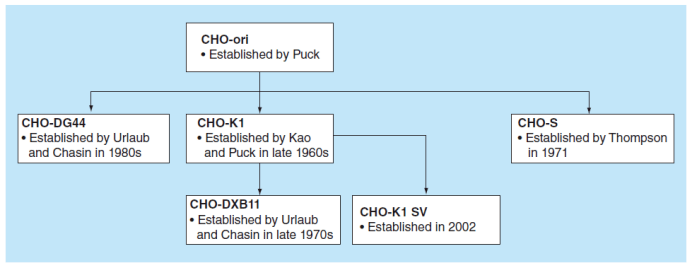
CHO细胞系发展历史

常用CHO宿主细胞的谱系
2. 培养基开发策略
培养基的主要作用是促进和维持细胞的生长发育,其开发策略可以分为两类:自上而下和自下而上。自下而上的策略指的是,对培养基中各种单一营养成分的不同浓度造成其对细胞生长和对产物产生的不同影响进行考察。该策略需要耗费大量的时间进行大量的试验,进而着重考察的是每一个组分对细胞的影响。而自上而下的策略指的是将培养基分成许多个不同的亚型,针对各个亚型先进行筛选和组合,而后再进行组内的优化。但不论是通过自上而下策略、还是自下而上策略开发出的培养基,通常都是需要和补料培养基一起进行使用的。
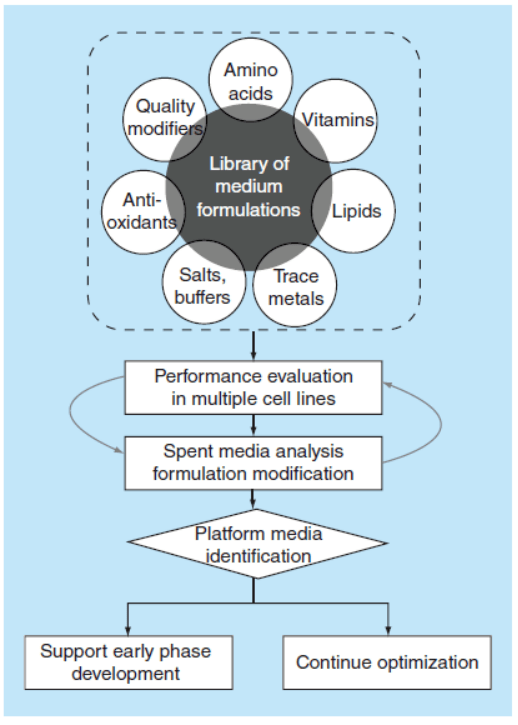
培养基开发流程图
以培养动物细胞为主的生物制药规模的不断扩大与生产成本高、产量低的矛盾不断加剧,培养基的优化设计成为了动物细胞表达产品产业化进程中的重要环节,也作为提高产量、降低生产成本的主要手段之一受到相关企业与研究机构越来越多的关注。典型的细胞培养方式有:批次培养、流加培养与灌注培养。批次培养是一种封闭的培养体系,因此营养物的消耗与代谢副产物的累积,往往会限制细胞生长及产物表达;流加培养,与灌注培养可以通过补充营养物和稀释副产物的方式减小这些限制,相对而说流加培养操作更简单灵活,目前细胞密度可达105-107,产物蛋白产量可达 10g/L 以上。
细胞培养基优化的基本步骤分为:
1 选择不同的培养基,进行单因素多水平测试,测试不同培养基对培养的影响;
2 对有机氮源进行氨基酸分析,这一步最好是由培养基提供商和制药商配合进行,或者请有符合认证的商业检测机构提供服务;
3 数据处理,根据不同培养基氨基酸水平,可以计算出每个测试中初始氨基酸的组成,然后再使用方差分析,计算每种氨基酸对培养结果的影响。
4 验证,如果方差分析结果显示某种或某些氨基酸是关键因素,则可以通过添加或稀释或混合使这些氨基酸达到优化的含量,然后经过测试,确定优化配方。
对基础培养基、流加培养基及灌注培养基的开发、优化已逐渐成为动物细胞培养产业化的关键一环,吸引了越来越多相关企业与研究机构的关注。目前已有多种细胞能够实现无血清培养,并且有多种无血清培养基也已经商业化各大培养基厂商都在不断推出新的培养基,以满足正在发展迅速的生物药厂;而各大药厂都在根据自己所培养的细胞类型寻找和开发与之相适应的培养基。与根据自身细胞类型进行培养基配方定制研究相比,采用现有商业化培养基进行细胞培养的优化显得更加方便和迅速。
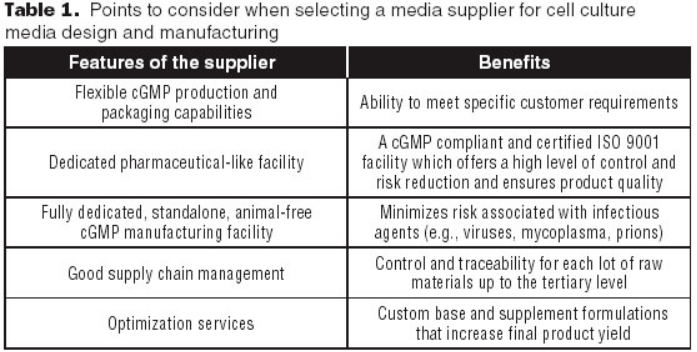
选择细胞培养基设计和制造的供应商时应考虑的要点
近些年来,灌流技术越来越多地应用于扩种或生产,这样做的目的是改善细胞生长和蛋白产率,提高反应器的使用效率并降低了成本。灌流可不断清除含有毒代谢副产物的培养基,同时以相似的速度不断补充新鲜培养基,如果灌流培养基设计得当,灌流过程中的营养消耗和生长抑制问题可被基本被抵消,如下图:
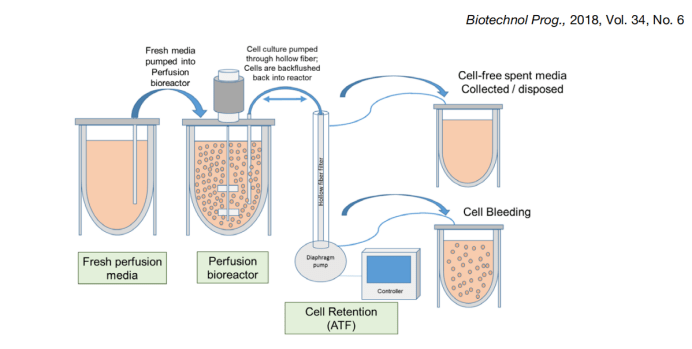
与传统的批处理的培养过程相比,细胞培养基和灌注条件决定了灌注培养的性能优劣,从而决定了最终产品的产量和产品质量。细胞灌注培养的设计目的是改善细胞的高生长和高生产力,寻找合适的培养条件(培养基粘度,少泡沫,适当的氧气溶解度,pH,渗透压等)非常重要。科研人员开发了各种类型的个性化培养基和灌流培养条件,用于上游培养加工中的多个步骤。如今,广泛的基础培养基和不同的灌流培养条件可用于获得均衡的碳水化合物,氨基酸,脂质,维生素,有机酸和微量元素用于目的产物的生产。
3.总结
未来五到十年培养基的发展将受到药物需求、制造过程、发展战略和设施的选择等方面共同的选择。生物制药制造商正在考虑模块化的设备,具有即插即用的功能设计。这种灵活性的概念是支持个性化药品,小批量生产,分散单一制造地点,启用模块化生产形式在区域范围内的部署,允许频繁使用新技术,在不干扰其他模块的情况下引入、实施新的工艺流程。改进的模块化能够支持多产品制造,最大化设施容量和降低总体成本。隨着对药物生产过程与质量一致性要求的不断提高、组学分析技术的快速发展和数据分析技术的不断创新,生物制药企业面对的研发成本高、生产周期长、实验数据复杂、规模放大等难题将得到更多的探索和逐渐的解决。
参考文献:
[1] Hu Z, Guo D, Yip SSM et al. Chinese hamster ovary K1 host cell enables stable cell line development for antibody molecules which are difficult to express in DUXB11- derived dihydrofolate reductase deficient host cell. Biotech Progress 29, 980–985 (2013).
[2] Zhu J. Mammalian cell protein expression for biopharmaceutical production. Biotechnol. Adv. 30, 1158–1170 (2012).
[3] Zhang H, Wang H, Liu M et al. Rational development of a serum-free medium and fed-batch process for a GS-CHO cell line expressing recombinant antibody. Cytotechnology 65, 363–378, (2013).
[4] Vargas Arigony AL, de Oliveria IM, Machado M et al. The influence of micronutrients in cell culture: a reflection on viability and genomic stability. BioMed. Res. Int. 2013, 1–22 (2013).
[5] Schaub J, Clemens C, Kaufmann H, Schulz TW. Advancing biopharmaceutical process development by system-level data analysis and integration of omics data. Adv Biochem Eng Bio technol. 2012;127:133–163.
[6] Dorai H, Liu S, Yao X et al. Proteomic analysis of bioreactor cultures of an antibody expressing CHO-GS cell line that promotes high productivity. J. Proteomics Bioinform. 6, 98–108 (2013).
[7] Hossler P, Racicot C, McDermott S. Targeted shifting of protein glycosylation profifiles in mammalian cell culture through media supplementation of cobalt. J Glycobiol. 2014;3:1.
附件