服务热线
178 0020 3020
在过去的几十年里,细胞治疗已经成为治疗恶性肿瘤非常有前景的方法,通过这些治疗,嵌合抗原受体(CAR)修饰的T细胞治疗已经被证实在血液肿瘤中有非常好的疗效。病人自体来源的或者供者异体来源的T细胞经修饰后表达CAR。这种CAR是嵌合结构,包含至少1个T细胞受体信号区域,以及一个单链抗体可变区(scFv)。
自体CART的制备过程包括一些基本的步骤。首先,病人的白细胞(WBCs)通过血细胞去除法分离后洗涤获得。然后,T细胞被激活,转导CAR基因,扩增到一定数量后灌装和密封后用于治疗。经过一定质控,患者经过预处理后,将CART细胞注射到患者体内。
尽管在目前的细胞治疗开发过程中,基本的开发方法类似,但在整个生产过程中依然有很多不同的过程。在早期临床试验中,目标细胞数量还没有被确认,因此这种工艺参数尚未被建立。此外,细胞扩增的能力在不同的病人,不同的工艺之间不同。据估计,按照目前的生产制造方法,CART的花费大概在$150000-30000之间。然而诺华的Kymriah花费大约是每个病人$475000。因此认识目前的主要工艺过程花费以及未来的制造策略非常重要。
本文总结了CART细胞治疗生产过程,主要考虑到过程参数以及经济学。通过调查目前发表的临床方面的数据来分析细胞治疗产品的制造过程。
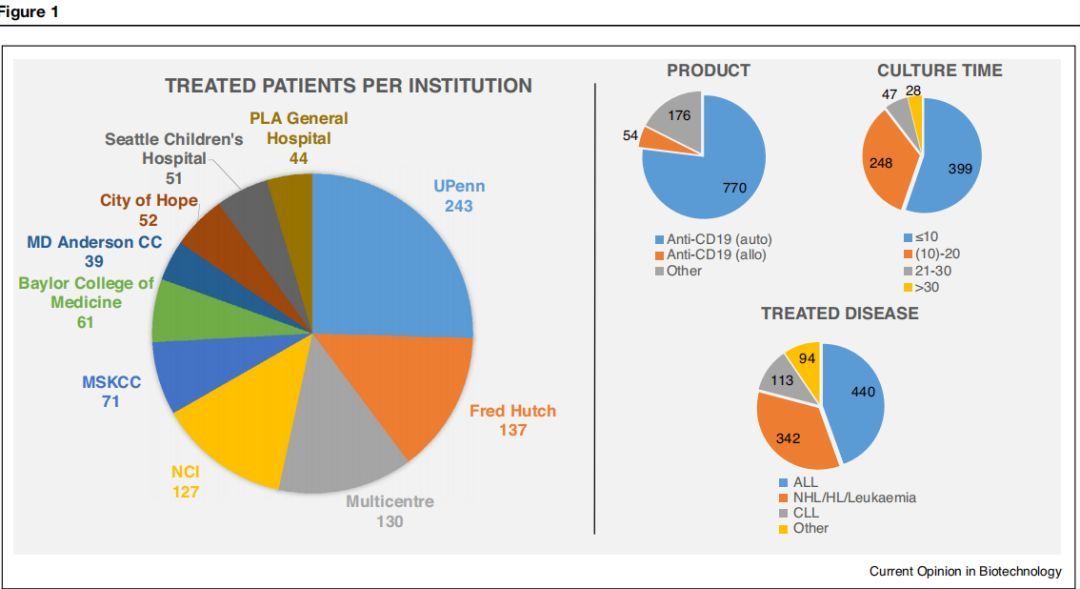
临床上已经发表的产品的技术参数
许多处于临床I和II期的疗效非常不错,且Kymriah和Yescarta的已经获批。但是,研究者们仍然没有开发出一个成熟的,完全可被接受的工艺过程,许多CART产品使用人工操作,非常耗时耗力,而且难以扩大,且失败率很高。产品开发过程中有许多基本步骤,如下:
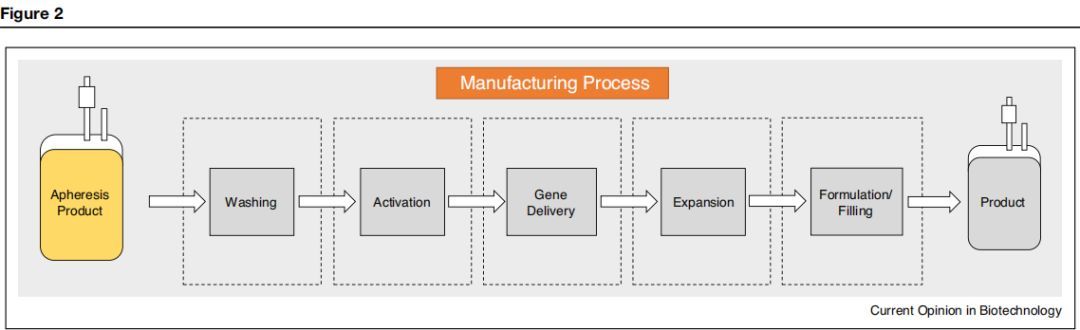
红细胞去除,细胞洗涤以及扩大培养
红细胞去除以及细胞洗涤
T细胞治疗流程中首先从病人的WBCs中将血细胞去除,通常采用连续或者半连续的密度梯度离心方法。
在分离的过程中需要加入抗凝剂,红细胞和血小板作为杂质在洗涤的过程中被清除。抗凝剂在活化的过程中能够改变细胞的特征,红细胞会影响产品的临床效果,血小板会导致细胞的聚集。为了去除红细胞和血小板,通常采用Ficoll密度梯度离心法。或者采用自动化的细胞洗涤机器例如COBE2991 Cell Processor,Haemonetics CellSaver, Baxter Cytomate, BiosafeSepax II 或者CaridianBCTElutra,洗涤后,直接使用WBCs或者WBCs经程序降温冷冻保存。
富集细胞
一些研究者使用CliniMACS系统对细胞进行富集和洗涤,在这一系统中连接有相对应的顺磁性抗体。FredHutchinson Cancer研究中心和西雅图儿童医院从WBCs中分离CD4+(Thelper细胞)和CD8+细胞(细胞毒T细胞)以回输一定比例的CD8+/CD4+细胞。类似的,Brown等富集收集CD62L+细胞。MDAnderson癌症中心发现NK细胞会阻碍T细胞的培养。当NK细胞超过10%时,使用CD56+磁珠可以去除NK细胞。
活化
在体内,天然的T细胞能够通过抗原呈递细胞例如DCs细胞进行刺激增殖和活化。T细胞受体(TCR)和位于DC细胞表面的主要组织相容复合物通过共刺激分子CD28,4-1BB和OX40进行T细胞的活化。为了避免和DCs细胞的复杂的共培养,研究者们使用许多方法来模拟天然T细胞的活化。
单克隆抗体和白介素
最基本的活化办法是添加OKT3(抗CD3抗体)和白介素(IL-2)。将人外周血单个核细胞(PBMCs)与淋巴瘤细胞进行共培养也是一种快速扩增的方法。IL-2的浓度在不同的实验中有所不同。Gattinoni等认为使用IL-2,尤其是过量的IL-2会导致T细胞耗尽,从而失去了T细胞的功能,效应功能丧失且很快会凋亡。Barrett和Ghassemi等发现使用IL-7和IL-15替代IL-2能够获取更高比例的记忆细胞亚群。
细胞尺寸大小的抗CD3/CD28磁珠
Kalos等使用抗CD3/CD28抗体磁珠做为一种人工抗原呈递微粒比起OKT3/IL-2有更好的活化记忆细胞的能力。这些磁珠的直径大约是4.5微米,能够使用电磁铁去除,最终使得每3*106个细胞中有不到100个残留磁珠。在扩增过程中,使用磁珠刺激比起使用anti-CD3和IL-2刺激细胞能够获取10-100倍高的细胞因子。附着有抗体的磁珠有许多优势,细胞培养和富集很容易实现,这些磁珠可以用来选择和活化细胞而不用去除掉直到细胞被收获。在灌流或者换液过程中可以避免损失掉这些磁珠上的抗体。研究表明,使用anti-CD3/CD28比起OKT3(anti-CD3单抗)和IL-2能更有利于T细胞存活。
人工抗原呈递细胞
在最近的临床研究中,CART细胞被没有生命活力的抗原呈递细胞活化,例如k562细胞系,表达相关刺激分子以及肿瘤相关抗原(TAA),辐射过的或者没有增殖能力的细胞符合现在的cGMP准则。它们不表达人白细胞抗原A和B,且选择性地刺激针对肿瘤抗原的CART。为了再生含有EBV特异性的TCRCAR T细胞,EBV被转化成LCL用于活化。
临床中的活化
我们调查了不同的生产工艺下的临床试验。文章统计了2002年到2017年9月的数据,细胞治疗产品类型和制造工艺不明的病人除外。
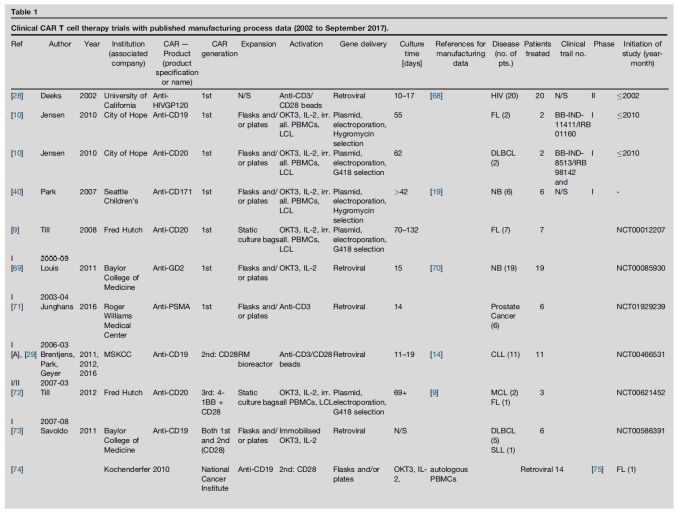
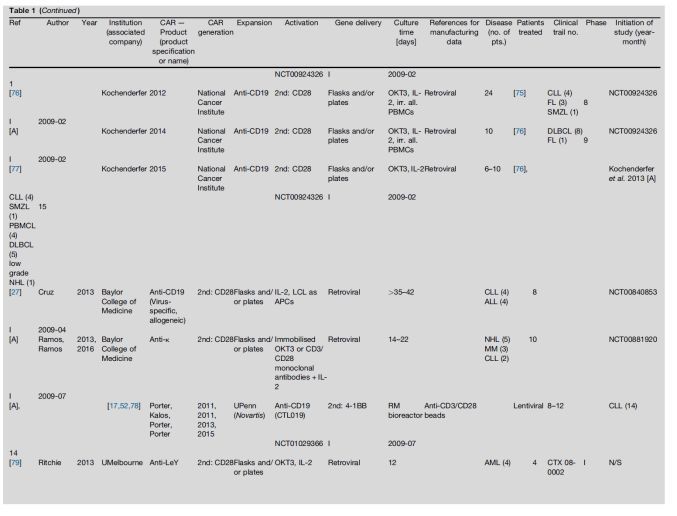
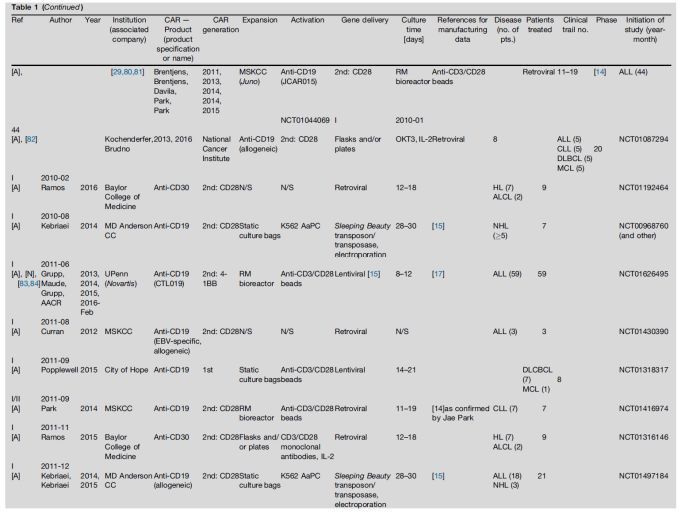
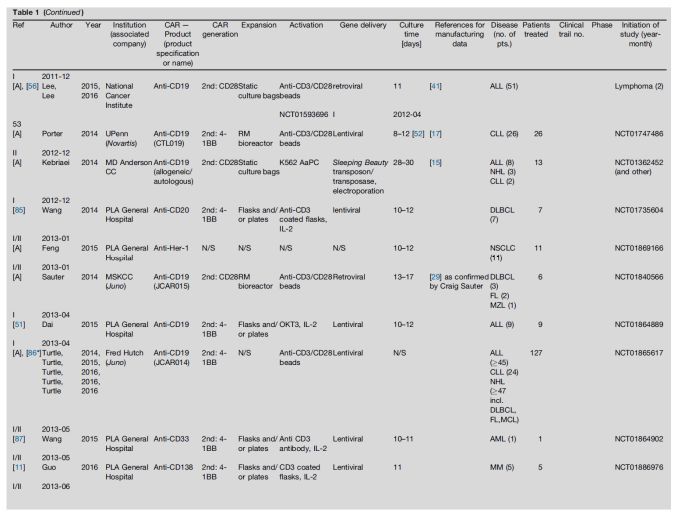
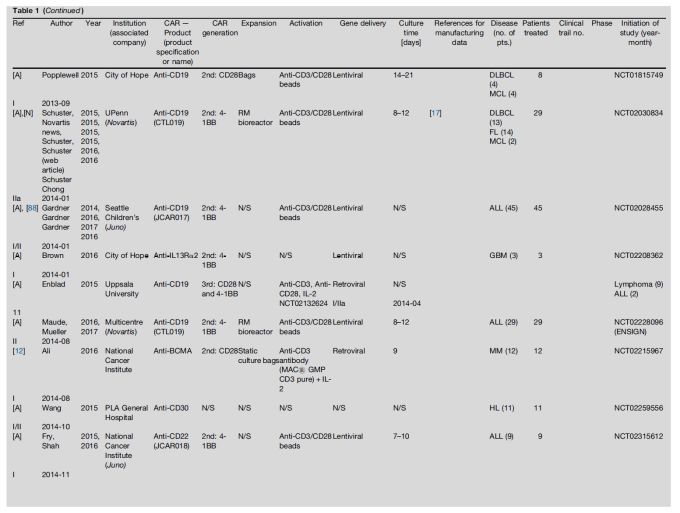
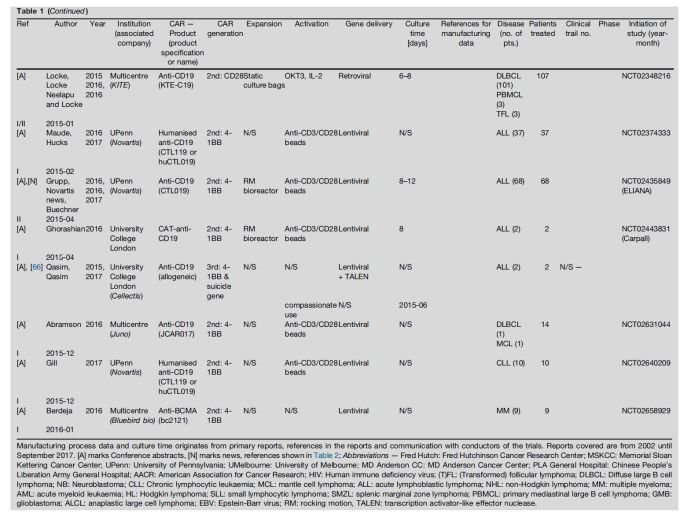
在952个可评估的临床试验中,626个试验通过添加抗CD3/CD28免疫磁珠的方法进行活化,279个通过抗CD3/CD28单抗和IL-2进行活化,其中有107个是KITE公司的KTE-019(已经被批准上市的Yescarta)。
基因转导
基因转导可以分为病毒和非病毒的方法。在CART细胞治疗中,包括电转DNA,转座子系统以及病毒载体,尤其是慢病毒或逆转录病毒转染。
病毒转染
逆转录和慢病毒基因转导方法具有较高的转染效率(约为4-70%),但显著地比质粒转导方式要贵。使用慢病毒或者逆转录病毒高效转染方法需要活化T细胞。尤其是在逆转录病毒转染过程中,转染能促进分裂细胞,细胞增殖能促进基因传递。在两种病毒转染方式中,都有癌症基因插入的风险,然而使用慢病毒转染方式这一风险会降低。目前,在CART细胞治疗中还没有出现类似报道。
病毒基因的制造需要在cGMP的环境中包装293T细胞系。这是一个费力且昂贵的步骤,主要是因为载体需要在洁净室中包装,且载体需要额外的放行检测。慢病毒的制造主要通过瞬时转染大量的质粒DNA;因此它的成本比起通过稳定包装细胞系的逆转录病毒要贵。开发稳定的包装细胞系,例如WinPac,能够降低慢病毒载体的制造成本。而且,病毒载体需要进行可复制病毒的检查,每个病人要花费数万美金。
质粒基因转导
使用转座子或者转座酶系统对CAR基因进行转导是一种比较新的方法。转座子是一段DNA序列能够通过转座酶切割和插入。CAR基因序列可以插入到质粒的转座子上。质粒在T细胞活化之前电转到T细胞中,之后转座酶切割含有CAR的转座子,然后插入到T细胞的基因组中。使用转座子系统比起电转方式能够改善基因转染的效率,转染效率接近病毒转染。
睡美人(SB)系统已经应用于CART细胞的制备。这种基因传递的方式不需要像临床慢病毒生产需要可重复生产,而且价格相对较低。但是这种基因转染方式的一个明显的缺陷就是生产出足够数量的应用于治疗的细胞所需要的时间较长。作为病毒基因转染方式,插入的基因有可能致癌或是引起其他相关基因的毁坏。然而,在最近的研究发现通过睡美人基因转染方式转染T细胞的方法比起病毒转染和piggyBac转座子/转座酶系统的致癌率要低很多。而且,SB转座子/转座酶系统制备的CART细胞在临床上已经有很好的前景。
目前临床试验中的基因转染方式
在978项数据完整的CART制备中,919项是病毒转染方法。其中521项是慢病毒转染产品,逆转录病毒是第二大转染方法,有398项。这两种方法均有较高的转染效率,较为安全但是价格昂贵。早期研究结果表明,简单的质粒DNA转染方式的临床效果稍差。转座子/转座酶系统也是最近才进入到临床研究中,已治疗了39名病人。如果这种转染方式被证实是安全有效的可行的,那么这一方法将被用于CART制备,是因为它比起病毒转染方式更经济。
扩增
T-Flasks 和静态细胞培养袋
在转导或转染的CART细胞扩增过程中,培养体积是变化的,通过增加培养容器的体积或者增加细胞培养方平的个数来增加培养的细胞量。这是非常耗力的,因为这些瓶子需要在受过专业训练的人在洁净室或者生物安全柜中进行操作。使用方平或者摇瓶不适用于大量细胞生产,是由于这些培养体系都是开放式的不适用于产业标准化的操作。静态培养袋子广泛应用于细胞的扩增,通过一些管路进行无菌连接。Tumaini等开发了一种半封闭的系统通过将静态细胞培养袋子之间连接起来后最小化开放系统。静态培养袋子易于操作,且比起组织培养皿更利于生产,由于细胞和培养基的传代和换液需要更少操作,因此更加安全。
摇摆式生物反应器
摇摆式生物反应器(RM)(例如:WAVE生物反应器/Xuri细胞培养袋子系统)可以通过灌流系统压缩操作空间。灌流体系能消除生长抑制物以保证连续的营养供给,以确保在静态培养袋子中培养体积最小。Sadeghi等发现摇摆生物反应器在培养TILs细胞时比起静态系统能够减少33%的工作量,培养基消耗减少50%。有趣的是,实验结果已经证实摇摆生物反应器能够使得最终培养体系中的CD4+细胞更多。放大培养是生物反应器的一个挑战,反应器中转轴的损坏会导致培养失败。这种Xuri系统能够实现半连续的自动化培养。
临床试验中的扩增
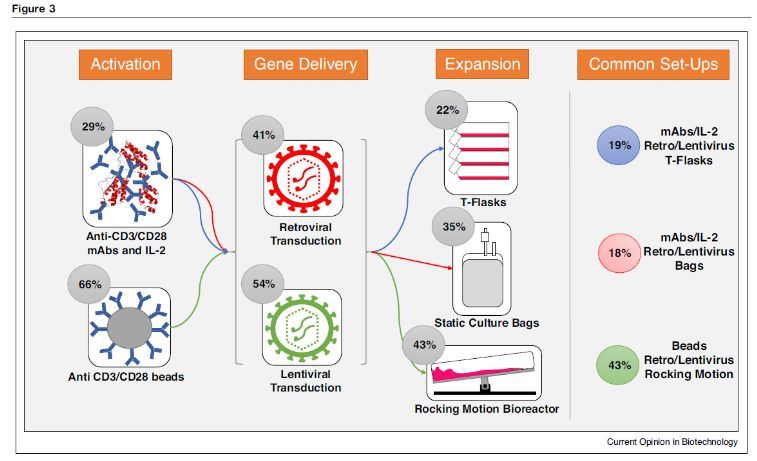
在目前的细胞培养过程中,培养体积的增加主要通过增加培养袋子或者摇瓶的体积来实现,或者将培养体系从平板变为摇瓶,从摇瓶到细胞培养袋子,从细胞培养袋子到生物反应器。这种细胞培养扩增方式可以分为三类。第一,679个CART产品中有295个使用磁珠活化,病毒转染,在摇摆式生物反应器中进行扩增,是最主要的培养方式(CTL019,JCAR014,JCAR017和JCAR018主要采纳这种方式)。有129种产品采用第二种培养方法,使用单克隆抗体/IL-2活化细胞,经病毒转染后在摇瓶中进行扩增,这种方法是一种手动操作的方法,是一种非自动化的策略。第三种最常见的培养方式是结合磁珠活化,病毒转染后使用静态培养袋子进行培养(有119种产品,占比为18%)。分析表明所有的细胞培养过程周期不超过20天。
CAR-T细胞生产过程种的挑战和新的解决方案
信使RNA转导以及其他的控制CAR功能的方法
脱靶毒性是临床种最为致命的风险。为了缓解mRNA转染过程的风险,研究者将CAR以瞬时转染的方式转入细胞以限制CAR的毒性。mRNA的多次转染方法能有效的诱导病人的抗肿瘤活力。另外,药物依赖的”杀伤基因“能够诱导自体凋亡,有效的缓和长期的脱靶毒性例如CD19-CARs导致B细胞再生障碍。这种方法被应用于NCT02028455临床实验中,T细胞被转染了CAR和EGFRt基因。
可变性以及缺乏确定的工艺参数是最大的技术挑战
目前有许多工艺方法,引起终产品的特性不同。另外,每个病人最初的血样不同。Brentjens等发现10个病人的CART的扩增倍数在23.6-385之间。有趣的是,最大和最小扩增倍数的培养时间差不多。23.6倍的扩增天数是18天,而385倍的扩增倍数在16天。最终的CART细胞数分别为1.1*109或者1.4*109。扩增倍数的不同说明了不同病人的细胞特性差异非常大。而且差异还显现在转导效率上,研究中表明逆转录病毒的转染效率在4-70%之间。Guo等发现慢病毒的转染效率在5.5%-45.3%之间,其他研究小组的数据也比较相似。这些内在的特征使得各研究和生产平台之间很难进行比较。还需要注意的是不同研究之间CAR的设计不同。关于CAR详细的设计Sadelain,Brentjens和Riviere在2013年时,Abate-Daga和Davila在2016,Jaspers和Brentjens等在2017年均已经报道过。
在临床研究中,CART细胞的剂量变化差异较大。最近临床效果不错的研究细胞的剂量均在106-107cells/kg的使用剂量(Sauteret al,2014, Park et al, 2013,2015。Schusteret al,2015a)。Lee等报道了在两个ALL病人,临床试验中接受了比计划剂量低的细胞。2号病人接受了0.03﹡106CAR T cells/kg,而5号病人接受了0.48*106CAR Tcells/kg,而不是预计的1-3*106CAR T cells/kg。2号病人疾病比较稳定,5号病人获得了完全缓解。有趣的是,2号和5号病人循环血液中CART细胞的数量没有明显的差异,说明,注射比预期要低的剂量的CART理论上是有效的,只要注射后有足够的扩增效率。
CAR-T细胞QA和QC
目前发表的一些关于安全,纯度和可行性的检测均依赖于cGMP原则。放行标准中,要求细胞无菌,缺乏可复制的病毒(如果是采用病毒转染)。可复制的慢病毒或者逆转录病毒一般采用基于细胞的方法或者qRT-PCR的方法。在美国CFR( Code of Federal Regulation)关于生物产品标准(21CFR610)中,要求无菌检测使用培养法或非培养法均可。培养法是基于细胞培养液和待检测材料共孵育后观察是否有获得微生物生长。Gram染色方法是一种非培养的检测方法。细胞和基因治疗是进展非常快的领域,需要从业者紧密跟踪法规要求。
理想的就是,产品的纯度要高,改善和去除特有的细胞类型能确保最初的原材料有较高的纯度。这也有利于检测污染的细胞类型,例如NK细胞。其他杂质包括过程中的内毒素,支原体或者残留,例如,残留的磁珠会有害,进入人体后会活化病人体内内源性的T细胞。
CART产品是通过检测转导效率和体外的杀伤毒性来证明是否有效的。CART细胞中的载体拷贝数是转导效率的一个指标。然而,这种基因拷贝数并不能完全反应CAR的表达。CAR阳性细胞可以通过最终产品的免疫表型表征来检测。为了检测CAR,研究者转导了一个tag到转基因载体上或者开发了CAR特异性的mAbs。一些研究中心做了体外细胞毒性的分析。例如,通过chromium释放的方法,这在终产品检测时需要花费时间。Singh等使用0.5*106个T细胞做chromium释放的方法来检测终产品。尽管这些方法适用于T细胞的检测,但是并没有一种标准方法,因此很难比较不同研究者或者不同平台之间的CART细胞。到目前为止杀伤效力分析是CART产品QC评估中最大的挑战。这主要是源于CART细胞的复杂性以及缺乏相应的标准方法。
生产-展望
单克隆抗体的商业化生产阶段可以进行批培养,获得很大剂量的单克隆抗体。这种规模在细胞治疗领域还没有实现。目前,自体小规模的血液瘤治疗占主要部分。尽管一些异体的CART产品已经进入临床,还需要考虑GvHD副作用。目前异体治疗的疗效不如自体治疗,目前一些研究通过基因编辑的方法来缓和GvHD,例如使得TCRα和β链基因失活。
第一个获批的CART产品是治疗急性淋巴细胞白血病(ALL)的Kymirah。而且是临床中治疗过最多的一种疾病(每1000个病人中有440个),尽管它只占USA,UK和德国癌症的0.4%。如果细胞治疗在肺癌和胰腺癌上也有疗效,将还会有一大批产品上市。
制备自体细胞产品对于制药行业是一个非常大的挑战。增加单个产品的产品线被称为是scaling-out。自动化的细胞治疗设备可以生产出大量的个性化的CART产品。Mock等使用美天旎的CliniMACSProdigy,一种自动化的细胞生产平台,能够生产出相关数量的CD19-CART。研究发现这种自动化的设备比起摇摆式生物反应器能大大减少人为操作。这种经济的,基础的,可调控的设备可以分布在医院进行细胞生产,但仍需和集中化的生产模式进行比较。
结论
细胞和基因治疗,尤其是CART,是一个非常振奋人心的方向,它们为许多疾病的治愈提供了可能。但是仍然有很多人担忧高额的成本和高度可变的制造过程。这里,我们分析了1000个用了CART治疗的病人。虽然都有相似的生产过程,进一步阐述了三个主要过程以及工艺规模,相关的剂量。目前为止,多数临床试验使用现成的仪器设备,来最小化批次之间的差异以及产品的费用。将来的趋势是会出现许多新的设备来提供自动化生产,以及封闭的生产体系来降低生产的费用。
参考文献:
Roddie C, O'Reilly M, Dias Alves Pinto J, Vispute K, Lowdell M.Manufacturing chimeric antigen receptor T cells: issues and challenges.Cytotherapy. 2019 Jan 23. pii: S1465-3249(18)30701-1
附件